由于格式問(wèn)題此試題可能會(huì)出現(xiàn)亂碼的情況
為了方便您閱讀請(qǐng)點(diǎn)擊右上角的全屏查看
2018南充市中考化學(xué)沖刺試題
一、選擇題
1.在化學(xué)實(shí)驗(yàn)中必須注意安全操作
①在點(diǎn)燃H2、CO、CH4等易燃?xì)怏w前,必須檢驗(yàn)氣體的純度
②在稀釋濃硫酸時(shí)將濃硫酸沿器壁慢慢注入水中,并用玻璃棒攪拌
③濃硫酸不慎滴到皮膚上,應(yīng)立即用大量水沖洗,再用3﹣5%的NaHCO3溶液涂上
④給試管中液體加熱,液體一般不超過(guò)試管容積的![]()
⑤稱量任何固體藥品時(shí),均要在天平的左右托盤(pán)上放等大的相同的紙片
上述說(shuō)法中錯(cuò)誤的是( )
A.③④????????????? B.②④????????????? C.①②③④????????????? D.⑤
2.下列實(shí)驗(yàn)中得到的數(shù)據(jù)或說(shuō)法正確的是( )
A.用托盤(pán)天平稱量了17.5g的氯化鈉
B.用量筒量取9.25mL的水
C.用pH試紙測(cè)定某地下水的pH是7.1
D.測(cè)定某溶液的pH時(shí),先將試紙用蒸餾水濕潤(rùn),再用玻璃棒蘸取待測(cè)液滴到置于白瓷板上的pH試紙上,半分鐘內(nèi)與標(biāo)準(zhǔn)比色卡對(duì)照即可
3.用“王水”(濃鹽酸與濃硝酸的混合物)溶解黃金后得到一種物質(zhì):HAuCl4(四氯合金酸),其中金元素(Au)的化合價(jià)為( )
A.+1????????????? B.+2????????????? C.+3????????????? D.+4
4(南充市中考化學(xué)).下列化學(xué)方程式不正確的是( )
①2H2O![]() H2+O2?? ②2Fe+6HCl=2FeCl3+3H2↑
H2+O2?? ②2Fe+6HCl=2FeCl3+3H2↑
③3CO+Fe2O3![]() 2Fe+CO2↑ ④H2+CuO
2Fe+CO2↑ ④H2+CuO![]() Cu+H2O
Cu+H2O
⑤Cu+ZnCl2=CuCl2+Zn ⑥Mg(OH)2+CuCl2=Cu(OH)2↓+MgCl2.
A.①②③④⑤????????????? B.②④⑤⑥????????????? C.①②⑤⑥????????????? D.①②③⑤⑥
5.用I2O5可以測(cè)定空氣污染的程度,發(fā)生的化學(xué)反應(yīng)為I2O5+5CO→I2+5CO2,其中氧化劑是( )
A.I2O5????????????? B.CO????????????? C.I2????????????? D.CO2
6. 2001年8月,科學(xué)家用單分子碳納米管制成了世界上最小的邏輯電路.納米碳管是一種由碳原子構(gòu)成的直徑約為幾納米(1納米=10﹣9米)的空心管,下列說(shuō)法錯(cuò)誤的是( )
A.碳納米管材料在一定條件下易將CO2還原成CO
B.碳納米管材料表面積大能使有色溶液褪色
C.碳納米管材料是一種特殊的有機(jī)化合物
D.碳納米管和金剛石、石墨在一定條件下在氧氣中完全燃燒產(chǎn)物相同
7.在抗擊“非典型肺炎”的戰(zhàn)斗中,常用濃度0.04%﹣0.5%的過(guò)氧乙酸溶液做各種預(yù)防消毒的消毒液,其化學(xué)式為:CH3COOOH,在配置過(guò)氧乙酸溶液的過(guò)程中,若量取水時(shí)仰視.(其他過(guò)程均正確),則結(jié)果所得溶液濃度( )
A.偏大????????????? B.偏小????????????? C.無(wú)影響????????????? D.無(wú)法確定
8.西班牙瑞奧汀河是一條酸河,經(jīng)調(diào)查發(fā)現(xiàn)是由于上游河床含有的物質(zhì)R在水中氧的作用下發(fā)生反應(yīng)所致,其反應(yīng)的化學(xué)方程式是:2R+2H2O+7O2═2H2SO4+2FeSO4則R的化學(xué)式是( )
A.FeS????????????? B.Fe2S3????????????? C.FeO????????????? D.FeS2
9.自來(lái)水生產(chǎn)中通常使用少量的氯氣進(jìn)行消毒,氯氣與水反應(yīng)的產(chǎn)物之一是鹽酸,市場(chǎng)上有些不法分子高牟取暴利,用自來(lái)水冒充純凈水出售,為辨別真?zhèn)危捎脕?lái)鑒別的( )
A.酚酞????????????? B.BaCl2????????????? C.NaOH????????????? D.AgNO3
10.將質(zhì)量分?jǐn)?shù)為60%的乙醇溶液(密度小于1)與等體積的水混合后,則所得溶液的溶質(zhì)質(zhì)量分?jǐn)?shù)為( )
A.等于30%????????????? B.大于30%????????????? C.小于30%????????????? D.等于35%
11.下列物質(zhì)中分別與AgNO3、K2CO3、CuSO4三種溶液混合,均有白色沉淀生成的是( )
A.鹽酸????????????? B.Ca(NO3)2????????????? C.NaOH????????????? D.BaCl2
12.能除去KNO3和NaCl混合液中所含有少量CuSO4和Fe2(SO4)3的一種試劑是( )
A.Ba(OH)2????????????? B.BaCl2????????????? C.AgNO3????????????? D.NaOH
13.為了驗(yàn)證Fe、Cu、Ag三種金屬的活動(dòng)性順序,現(xiàn)有所需金屬,如果只選一種鹽且實(shí)驗(yàn)最簡(jiǎn)單的是( )
A.AgNO3????????????? B.CuSO4????????????? C.FeSO4????????????? D.ZnCl2
14(南充市中考化學(xué)).工業(yè)鹽酸因含有FeCl3而顯黃色,現(xiàn)向1~2ml工業(yè)鹽酸中逐滴滴加NaOH溶液,其加入量(X)與生成沉淀量(Y)的關(guān)系應(yīng)是( )
A.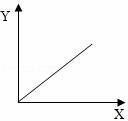 ????????????? B.
????????????? B. ?????????????
?????????????
C.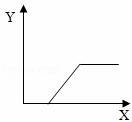 ????????????? D.
????????????? D.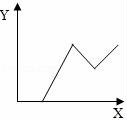
15.鐵有三種常見(jiàn)的氧化物:FeO、Fe2O3、Fe3O4.現(xiàn)有某鐵的氧化物樣品,已知其中鐵與氧質(zhì)量比是21:8關(guān)于該樣品的說(shuō)法正確的是( )
A.一定是純凈物
B.一定是混合物
C.不可能是Fe3O4和FeO組成的混合物
D.該樣品只有兩種情況,即只有Fe3O4或者是FeO、Fe2O3構(gòu)成的混合物
二、填空題
16.用符號(hào)表示:(1)兩個(gè)亞鐵離子 ;(2)3個(gè)硫酸分子 .
17.硒元素具有抗衰老,抑制癌細(xì)胞的功能,它的化學(xué)性質(zhì)與硫相似,元素符號(hào)為Se,它對(duì)應(yīng)的含氧酸的化學(xué)式是:H2SeO4,這種酸應(yīng)讀作 ,其與氫氧化鈉溶液反應(yīng)的化學(xué)方程式是 .
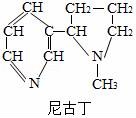
18.如圖為香煙中有害物質(zhì)尼古丁的結(jié)構(gòu)式(短線代表電子對(duì)),則該物質(zhì)的化學(xué)式為 ,該物質(zhì)的相對(duì)分子質(zhì)量為 .

19.蛋糕等食品包裝中的除氧劑是一種黑色粉末狀的固體,失效后帶有紅褐色.某化學(xué)課外興趣小組為了探究其主要成分,將一包未變質(zhì)的除氧劑分成兩份:一份加入稀鹽酸中,發(fā)現(xiàn)大量氣泡產(chǎn)生;另一份加入到氯化銅溶液中,一段時(shí)間后溶液顏色變淡綠色,固體逐漸變紅.請(qǐng)回答:
(1)該除氧劑的主要成份是 ;
(2)為了驗(yàn)證上述推斷是否正確,可以用到一種物理方法,即 .
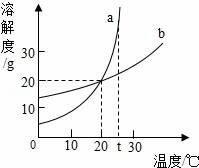
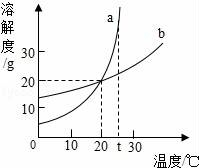
20.如圖是a、b兩種固體物質(zhì)的溶解度曲線,試回答:
(1)t℃時(shí),兩物質(zhì)的溶解度的大小關(guān)系:a b(填“大于”、“等于”或“小于”)
(2)當(dāng)a中含有 少量b時(shí),可以用 法提純a;
(3)a、b都屬于 物質(zhì);(填“難溶”、“微溶”、“可溶”、“易溶”)
(4)在 ℃時(shí)a、b的溶解度相等,此時(shí)150g水中最多可溶解物質(zhì) g.
21.(南充市中考化學(xué))現(xiàn)有一包白色固體混合物,可能由BaCl2、KNO3、CuSO4、FeCl3、Na2CO3、Na2SO4、NaCl等中的幾種混合而成,為證明其組成,做如下實(shí)驗(yàn):
①取一定量該固體混合物加入足量的水,充分?jǐn)嚢瑁玫桨咨恋砗蜔o(wú)色溶液.過(guò)濾得到白色沉淀A,無(wú)色濾液B.
②向白色沉淀A中加入過(guò)量的鹽酸溶液,沉淀部分溶解.
③向無(wú)色濾液B中加入硝酸銀溶液,產(chǎn)生不溶于稀硝酸的白色沉淀.
則:(1)該固體混合物中一定含有 ,可能含有 ,一定沒(méi)有 .(用化學(xué)式填空)
(2)該混合物至少由 種物質(zhì)構(gòu)成,該混合物的所有可能組合有 種(填數(shù)字).
三、實(shí)驗(yàn)題
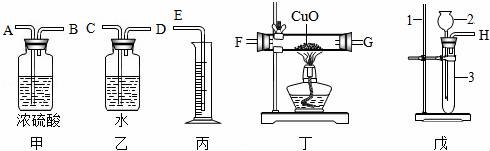
22.現(xiàn)有一定量的含ZnO的鋅粒,請(qǐng)從圖中選擇適當(dāng)?shù)膶?shí)驗(yàn)裝置,設(shè)計(jì)一實(shí)驗(yàn)測(cè)定鋅粒的純度,可供選擇的試劑有:①稀硫酸 ②稀硝酸 ③濃硫酸 ④硫酸銅溶液 ⑤濃硝酸.
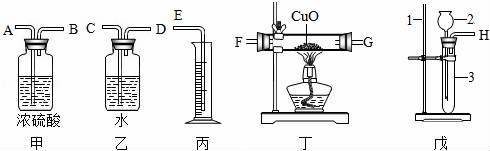
請(qǐng)回答下列問(wèn)題:
(1)寫(xiě)出儀器的名稱:1 2 3 ;
(2)測(cè)定純度可以設(shè)計(jì)兩種方法,一種是最簡(jiǎn)單的,則選擇儀器是 (填裝置編號(hào)).戊中選擇的藥品是 (填編號(hào));若氣體從左向右流,則接口的順序?yàn)椤 。ㄌ罱涌谧帜复?hào));
(3)儀器組裝好后,在開(kāi)始實(shí)驗(yàn)時(shí),要先 ,操作方法是 .
(4)若實(shí)驗(yàn)樣品質(zhì)量是10g,實(shí)驗(yàn)中測(cè)定氫氣的體積是2.22L(氫氣密度為0.09g/L)則樣品的純度為 .
四、計(jì)算題
23.某石灰廠新到一批石灰石,其中含有雜質(zhì)二氧化硅(二氧化硅不溶于水,不與鹽酸反應(yīng),高溫不分解)為測(cè)定石灰石樣品的純度,某化學(xué)研究性學(xué)習(xí)小組的同學(xué)分成三組實(shí)驗(yàn)測(cè)得數(shù)據(jù)如表:
實(shí)驗(yàn)次數(shù) | 1 | 2 | 3 |
稀鹽酸質(zhì)量(g) | 50 | 50 | 100 |
樣品質(zhì)量(g) | 20 | 30 | 20 |
剩余物質(zhì)質(zhì)量(g) | 63.4 | 73.4 | 113.4 |
產(chǎn)生氣體的質(zhì)量(g) | 6.6 | 6.6 |
|
(1)表格第3組空格中應(yīng)填寫(xiě)的數(shù)據(jù)是 ;
(2)該實(shí)驗(yàn)中,第 (填數(shù)字)組同學(xué)的實(shí)驗(yàn)中,稀鹽酸一定反應(yīng)完全;
(3)求出該石灰石樣品的純度. (請(qǐng)寫(xiě)出計(jì)算過(guò)程,否則不得分)
南充市中考化學(xué)參考答案與試題解析
一、選擇題
1.在化學(xué)實(shí)驗(yàn)中必須注意安全操作
①在點(diǎn)燃H2、CO、CH4等易燃?xì)怏w前,必須檢驗(yàn)氣體的純度
②在稀釋濃硫酸時(shí)將濃硫酸沿器壁慢慢注入水中,并用玻璃棒攪拌
③濃硫酸不慎滴到皮膚上,應(yīng)立即用大量水沖洗,再用3﹣5%的NaHCO3溶液涂上
④給試管中液體加熱,液體一般不超過(guò)試管容積的![]()
⑤稱量任何固體藥品時(shí),均要在天平的左右托盤(pán)上放等大的相同的紙片
上述說(shuō)法中錯(cuò)誤的是( )
A.③④????????????? B.②④????????????? C.①②③④????????????? D.⑤
【考點(diǎn)】HM:氫氣、一氧化碳、甲烷等可燃?xì)怏w的驗(yàn)純;43:稱量器﹣托盤(pán)天平;4B:給試管里的液體加熱;4D:濃硫酸的性質(zhì)及濃硫酸的稀釋;4M:常見(jiàn)的意外事故的處理方法.
【專題】531:常見(jiàn)儀器及化學(xué)實(shí)驗(yàn)基本操作.
【分析】①、根據(jù)可燃性氣體遇明火可能發(fā)生爆炸進(jìn)行解答;
②根據(jù)濃硫酸的稀釋是將濃硫酸倒入水且用玻璃棒進(jìn)行攪拌進(jìn)行解答;
③根據(jù)濃硫酸的處理方法解答;
④根據(jù)給液體加熱注意事項(xiàng)進(jìn)行解答;
⑤根據(jù)有腐蝕性的藥品需要放在燒杯中稱量進(jìn)行解答.
【解答】解:①、H2、CO、CH4屬于可燃性氣體,可燃性氣體遇明火可能發(fā)生爆炸,所以在點(diǎn)燃H2、CO、CH4等易燃?xì)怏w前.必須檢驗(yàn)氣體的純度,故正確;
②濃硫酸的稀釋是將濃硫酸倒入水且用玻璃棒進(jìn)行攪拌,故正確;
③濃硫酸不慎滴到皮膚上,應(yīng)立即用大量水沖洗,再用3﹣5%的NaHCO3溶液涂上,故正確;
④給液體加熱注意事項(xiàng):給試管中的液體加熱,液體一般不超過(guò)試管容積的![]() ,故正確;
,故正確;
⑤有腐蝕性的藥品需要放在燒杯中稱量,例如氫氧化鈉需要放在燒杯中稱量,故錯(cuò)誤.
故選:D.
【點(diǎn)評(píng)】學(xué)實(shí)驗(yàn)要嚴(yán)格遵守操作規(guī)程,否則會(huì)造成不良后果或危險(xiǎn);通過(guò)本題的解答,有利于培養(yǎng)學(xué)生的安全意識(shí)和嚴(yán)謹(jǐn)?shù)膶?shí)驗(yàn)態(tài)度.
2.下列實(shí)驗(yàn)中得到的數(shù)據(jù)或說(shuō)法正確的是( )
A.用托盤(pán)天平稱量了17.5g的氯化鈉
B.用量筒量取9.25mL的水
C.用pH試紙測(cè)定某地下水的pH是7.1
D.測(cè)定某溶液的pH時(shí),先將試紙用蒸餾水濕潤(rùn),再用玻璃棒蘸取待測(cè)液滴到置于白瓷板上的pH試紙上,半分鐘內(nèi)與標(biāo)準(zhǔn)比色卡對(duì)照即可
【考點(diǎn)】31:實(shí)驗(yàn)數(shù)據(jù)處理或者誤差分析的探究;42:測(cè)量容器﹣量筒;43:稱量器﹣托盤(pán)天平;4U:溶液的酸堿度測(cè)定.
【專題】16 :壓軸實(shí)驗(yàn)題;531:常見(jiàn)儀器及化學(xué)實(shí)驗(yàn)基本操作.
【分析】A、根據(jù)托盤(pán)天平正確讀數(shù)方法分析;
B、根據(jù)量筒正確讀數(shù)方法分析;
C、根據(jù)pH試紙的讀數(shù)方法分析;
D、根據(jù)pH試紙的使用方法進(jìn)行分析.
【解答】解:A、托盤(pán)天平是粗略的量器,能稱準(zhǔn)到0.1g,故A正確;
B、量筒是粗略的量器,能量準(zhǔn)到0.1mL,故不可以用量筒量取9.25mL的水,故B錯(cuò)誤;
C、用pH試紙測(cè)定pH值只能到整數(shù)位,不能讀出小數(shù)點(diǎn)后的值,故C錯(cuò)誤;
D、用pH試紙測(cè)定溶液的pH時(shí)的正確做法:撕一小段pH試紙置于表面皿中,用玻璃棒蘸取試液滴在pH試紙上,再與標(biāo)準(zhǔn)比色卡對(duì)照讀出pH值,不能將試紙用蒸餾水濕潤(rùn),故D錯(cuò)誤.
故選A.
【點(diǎn)評(píng)】本題主要考查化學(xué)儀器的讀數(shù)方法和使用情況,要求學(xué)生有良好的實(shí)驗(yàn)基礎(chǔ)和解決問(wèn)題的能力.
3.用“王水”(濃鹽酸與濃硝酸的混合物)溶解黃金后得到一種物質(zhì):HAuCl4(四氯合金酸),其中金元素(Au)的化合價(jià)為( )
A.+1????????????? B.+2????????????? C.+3????????????? D.+4
【考點(diǎn)】D6:有關(guān)元素化合價(jià)的計(jì)算.
【專題】191:化學(xué)式的計(jì)算.
【分析】根據(jù)在化合物中正負(fù)化合價(jià)代數(shù)和為零,進(jìn)行解答本題.
【解答】解:設(shè)HAuCl4(四氯合金酸)中金元素的化合價(jià)為x.由氫元素為+1價(jià),氯元素為﹣1價(jià),根據(jù)在化合物中正負(fù)化合價(jià)代數(shù)和為零,可得 (+1)+x+(﹣1)×4=0,解答x=+3;
故選:C.
【點(diǎn)評(píng)】本題考查學(xué)生根據(jù)在化合物中正負(fù)化合價(jià)代數(shù)和為零計(jì)算指定元素化合價(jià)的解題能力.
4.下列化學(xué)方程式不正確的是( )
①2H2O![]() H2+O2?? ②2Fe+6HCl=2FeCl3+3H2↑
H2+O2?? ②2Fe+6HCl=2FeCl3+3H2↑
③3CO+Fe2O3![]() 2Fe+CO2↑ ④H2+CuO
2Fe+CO2↑ ④H2+CuO![]() Cu+H2O
Cu+H2O
⑤Cu+ZnCl2=CuCl2+Zn ⑥Mg(OH)2+CuCl2=Cu(OH)2↓+MgCl2.
A.①②③④⑤????????????? B.②④⑤⑥????????????? C.①②⑤⑥????????????? D.①②③⑤⑥
【考點(diǎn)】G5:書(shū)寫(xiě)化學(xué)方程式.
【專題】513:化學(xué)用語(yǔ)和質(zhì)量守恒定律.
【分析】根據(jù)書(shū)寫(xiě)方程式要遵循的原則:必須以客觀事實(shí)為基礎(chǔ)、要遵守質(zhì)量守恒定律進(jìn)行判斷.
【解答】解:①反應(yīng)條件錯(cuò)誤,生成的氣體后面未標(biāo)↑,還沒(méi)有配平,正確的化學(xué)方程式為:2H2O![]() 2H2↑+O2↑;
2H2↑+O2↑;
②鐵與酸反應(yīng)生成的是亞鐵鹽,正確的化學(xué)方程式為:Fe+2HCl=FeCl2+H2↑;
③配平錯(cuò)誤,↑用錯(cuò),正確的化學(xué)方程式為:3CO+Fe2O3![]() 2Fe+3CO2;
2Fe+3CO2;
④該化學(xué)方程式完全正確;
⑤在金屬活動(dòng)順序表中,銅排在鋅的后面,故銅不能置換氯化鋅中的鋅,故錯(cuò)誤;
⑥堿和鹽反應(yīng)時(shí),二者必須都可溶,氫氧化鎂不溶于水,故二者不能發(fā)生反應(yīng);
故選D
【點(diǎn)評(píng)】在判斷方程式的書(shū)寫(xiě)是否正確時(shí),主要依據(jù)書(shū)寫(xiě)方程式的兩個(gè)原則.
5.(南充市中考化學(xué))用I2O5可以測(cè)定空氣污染的程度,發(fā)生的化學(xué)反應(yīng)為I2O5+5CO→I2+5CO2,其中氧化劑是( )
A.I2O5????????????? B.CO????????????? C.I2????????????? D.CO2
【考點(diǎn)】F5:氧化反應(yīng).
【專題】152:結(jié)合課本知識(shí)的信息.
【分析】氧化劑指的是反應(yīng)物,且在反應(yīng)中為其它物質(zhì)提供了氧,利用這一知識(shí)對(duì)反應(yīng)進(jìn)行分析探討即可.
【解答】解:在反應(yīng)I2O5+5CO→I2+5CO2中I2O5失掉了氧并為一氧化碳提供了氧使其變成了二氧化碳,因此I2O5是這一反應(yīng)的氧化劑.
故選A.
【點(diǎn)評(píng)】此題是對(duì)氧化劑概念及判斷的考查,解題的關(guān)鍵是知道氧化劑在反應(yīng)中的特點(diǎn),并結(jié)合實(shí)際的反應(yīng)進(jìn)行判斷,屬基礎(chǔ)性知識(shí)概念考查題.
6.2001年8月,科學(xué)家用單分子碳納米管制成了世界上最小的邏輯電路.納米碳管是一種由碳原子構(gòu)成的直徑約為幾納米(1納米=10﹣9米)的空心管,下列說(shuō)法錯(cuò)誤的是( )
A.碳納米管材料在一定條件下易將CO2還原成CO
B.碳納米管材料表面積大能使有色溶液褪色
C.碳納米管材料是一種特殊的有機(jī)化合物
D.碳納米管和金剛石、石墨在一定條件下在氧氣中完全燃燒產(chǎn)物相同
【考點(diǎn)】CA:碳元素組成的單質(zhì);AA:有機(jī)物的特征、分類及聚合物的特性;C7:碳的化學(xué)性質(zhì).
【專題】523:碳單質(zhì)與含碳化合物的性質(zhì)與用途.
【分析】A、根據(jù)碳的化學(xué)性質(zhì)考慮;B、根據(jù)結(jié)構(gòu)特點(diǎn)考慮;C、根據(jù)有機(jī)化合物的定義考慮;D、根據(jù)元素組成考慮生成物.
【解答】解:A、因?yàn)榧{米碳管是一種由碳原子構(gòu)成的單質(zhì),碳具有還原性,可以與CO2反應(yīng)生成CO,故A說(shuō)法正確;
B、碳納米管材料表面積大能將色素吸附在表面,所以能使有色溶液褪色,故B說(shuō)法正確;
C、有機(jī)化合物必須是含碳的化合物,納米碳管是一種由碳原子構(gòu)成的單質(zhì),故C說(shuō)法錯(cuò)誤;
D、碳納米管和金剛石、石墨都是由碳元素組成,在一定條件下在氧氣中完全燃燒產(chǎn)物都是二氧化碳,故D說(shuō)法正確.
故選C.
【點(diǎn)評(píng)】解答本題關(guān)鍵是要知道碳單質(zhì)的化學(xué)性質(zhì)和結(jié)構(gòu)特點(diǎn)決定它的性質(zhì).
7.在抗擊“非典型肺炎”的戰(zhàn)斗中,常用濃度0.04%﹣0.5%的過(guò)氧乙酸溶液做各種預(yù)防消毒的消毒液,其化學(xué)式為:CH3COOOH,在配置過(guò)氧乙酸溶液的過(guò)程中,若量取水時(shí)仰視.(其他過(guò)程均正確),則結(jié)果所得溶液濃度( )
A.偏大????????????? B.偏小????????????? C.無(wú)影響????????????? D.無(wú)法確定
【考點(diǎn)】4E:一定溶質(zhì)質(zhì)量分?jǐn)?shù)的溶液的配制.
【專題】192:溶液的組成及溶質(zhì)質(zhì)量分?jǐn)?shù)的計(jì)算.
【分析】運(yùn)用仰視量取的液體的體積比實(shí)際需要的水要多,配制的溶液質(zhì)量比實(shí)際所需配制的溶液質(zhì)量大,溶質(zhì)質(zhì)量分?jǐn)?shù)=![]() ×100%,所以溶質(zhì)質(zhì)量分?jǐn)?shù)偏小解答
×100%,所以溶質(zhì)質(zhì)量分?jǐn)?shù)偏小解答
【解答】解:仰視量取的液體的體積比實(shí)際需要的水要多,配制的溶液質(zhì)量比實(shí)際所需配制的溶液質(zhì)量大,溶質(zhì)質(zhì)量分?jǐn)?shù)=![]() ×100%,所以溶質(zhì)質(zhì)量分?jǐn)?shù)偏小.
×100%,所以溶質(zhì)質(zhì)量分?jǐn)?shù)偏小.
故答案選B.
【點(diǎn)評(píng)】量筒讀數(shù)要平視凹液面的最底部,不能仰視和俯視讀數(shù),仰視讀數(shù)偏小俯視讀數(shù)偏大;但若量取一定體積的液體仰視會(huì)使量取的液體的體積偏大,俯視偏小.
8.西班牙瑞奧汀河是一條酸河,經(jīng)調(diào)查發(fā)現(xiàn)是由于上游河床含有的物質(zhì)R在水中氧的作用下發(fā)生反應(yīng)所致,其反應(yīng)的化學(xué)方程式是:2R+2H2O+7O2═2H2SO4+2FeSO4則R的化學(xué)式是( )
A.FeS????????????? B.Fe2S3????????????? C.FeO????????????? D.FeS2
【考點(diǎn)】G1:質(zhì)量守恒定律及其應(yīng)用.
【專題】513:化學(xué)用語(yǔ)和質(zhì)量守恒定律.
【分析】由質(zhì)量守恒定律:反應(yīng)前后,原子種類、數(shù)目均不變,據(jù)此由反應(yīng)的化學(xué)方程式推斷反應(yīng)物R的化學(xué)式.
【解答】解:根據(jù)反應(yīng)的化學(xué)方程式2R+2H2O+7O2=2H2SO4+2FeSO4,反應(yīng)物中氫、氧原子個(gè)數(shù)分別為4、16,反應(yīng)后的生成物中氫、硫、氧、鐵原子個(gè)數(shù)分別為4、4、16、2,根據(jù)反應(yīng)前后原子種類、數(shù)目不變,則2R中含有2個(gè)鐵原子和4個(gè)硫原子,則每個(gè)R分子由1個(gè)鐵原子和2個(gè)硫原子構(gòu)成,則物質(zhì)X的化學(xué)式為FeS2.
故選:D.
【點(diǎn)評(píng)】本題難度不大,利用化學(xué)反應(yīng)前后元素守恒、原子守恒來(lái)確定物質(zhì)的化學(xué)式是正確解題的關(guān)鍵.
9.自來(lái)水生產(chǎn)中通常使用少量的氯氣進(jìn)行消毒,氯氣與水反應(yīng)的產(chǎn)物之一是鹽酸,市場(chǎng)上有些不法分子高牟取暴利,用自來(lái)水冒充純凈水出售,為辨別真?zhèn)危捎脕?lái)鑒別的( )
A.酚酞????????????? B.BaCl2????????????? C.NaOH????????????? D.AgNO3
【考點(diǎn)】93:酸的化學(xué)性質(zhì).
【專題】525:常見(jiàn)的酸 酸的通性.
【分析】根據(jù)氯氣會(huì)與水生成鹽酸,自來(lái)水中含有的鹽酸,鑒別純凈水真?zhèn)危瑢?shí)際上就是檢驗(yàn)氯離子的存在進(jìn)行分析.
【解答】解:A、鹽酸不會(huì)使酚酞變色,不能鑒別,故A錯(cuò)誤;
B、氯化鋇不會(huì)與鹽酸反應(yīng),不能鑒別,故B錯(cuò)誤;
C、氫氧化鈉會(huì)與鹽酸反應(yīng),但是無(wú)明顯現(xiàn)象,不能鑒別,故C錯(cuò)誤;
D、硝酸銀會(huì)與鹽酸反應(yīng)生成氯化銀沉淀,可以鑒別,故D正確.
故選:D.
【點(diǎn)評(píng)】本題考查了常見(jiàn)物質(zhì)的鑒別,在解此類題時(shí),首先分析需要鑒別的物質(zhì)的性質(zhì),然后選擇適當(dāng)?shù)脑噭霈F(xiàn)不同的現(xiàn)象即可鑒別.
10.將質(zhì)量分?jǐn)?shù)為60%的乙醇溶液(密度小于1)與等體積的水混合后,則所得溶液的溶質(zhì)質(zhì)量分?jǐn)?shù)為( )
A.等于30%????????????? B.大于30%????????????? C.小于30%????????????? D.等于35%
【考點(diǎn)】7U:有關(guān)溶質(zhì)質(zhì)量分?jǐn)?shù)的簡(jiǎn)單計(jì)算.
【專題】192:溶液的組成及溶質(zhì)質(zhì)量分?jǐn)?shù)的計(jì)算.
【分析】根據(jù)加水混合后溶液中溶質(zhì)的質(zhì)量不變,乙醇溶液與等體積的水混合后,所得乙醇溶液的質(zhì)量為原乙醇溶液質(zhì)量與所加水質(zhì)量和,所得乙醇溶液中溶質(zhì)為60%的乙醇溶液中溶質(zhì),利用溶液的溶質(zhì)質(zhì)量分?jǐn)?shù)計(jì)算式求出所得乙醇的質(zhì)量分?jǐn)?shù);其中需要使用m=ρV對(duì)體積進(jìn)行換算.
【解答】解:假設(shè)乙醇溶液與水的體積都為V,乙醇溶液的密度為ρ、水密度為1,
混合后所得溶液的溶質(zhì)質(zhì)量分?jǐn)?shù)=![]() ×100%=
×100%=![]() ,由于ρ小于1,所以
,由于ρ小于1,所以![]() 大于1,則1+
大于1,則1+![]() 大于2,所以
大于2,所以![]() 就小于30%∴所得溶液的溶質(zhì)質(zhì)量分?jǐn)?shù)小于30%.
就小于30%∴所得溶液的溶質(zhì)質(zhì)量分?jǐn)?shù)小于30%.
故選C.
【點(diǎn)評(píng)】根據(jù)加水稀釋時(shí)溶液中溶質(zhì)質(zhì)量不變的特點(diǎn),可由稀釋前后溶質(zhì)質(zhì)量相等完成稀釋類問(wèn)題的計(jì)算.
11.(南充市中考化學(xué))下列物質(zhì)中分別與AgNO3、K2CO3、CuSO4三種溶液混合,均有白色沉淀生成的是( )
A.鹽酸????????????? B.Ca(NO3)2????????????? C.NaOH????????????? D.BaCl2
【考點(diǎn)】9H:鹽的化學(xué)性質(zhì).
【專題】527:常見(jiàn)的鹽 化學(xué)肥料.
【分析】硝酸銀能與含氯離子的物質(zhì)結(jié)合成白色沉淀,硫酸銅能與含鋇離子的物質(zhì)結(jié)合成白色沉淀,碳酸鉀可以與含鈣離子或鋇離子的物質(zhì)結(jié)合成白色沉淀.
【解答】解:A、鹽酸與硝酸銀能反應(yīng)生成氯化銀白色沉淀,而與硫酸銅和碳酸鉀混合不能生成沉淀,故A錯(cuò)誤;
B、硝酸鈣與碳酸鉀能反應(yīng)生成碳酸鈣白色沉淀,而與硝酸銀和硫酸銅混合不能生成沉淀,故B錯(cuò)誤;
C、氫氧化鈉溶液與這三種物質(zhì)混合都不能生成白色沉淀,故C錯(cuò)誤;
D、氯化鋇溶液能與硝酸銀反應(yīng)生成氯化銀白色沉淀,與硫酸銅反應(yīng)能生成硫酸鋇白色沉淀,與碳酸鉀混合能生成碳酸鋇白色沉淀,故D正確,
故選D.
【點(diǎn)評(píng)】本題考查了常見(jiàn)物質(zhì)間的反應(yīng),完成此題,可以依據(jù)物質(zhì)的性質(zhì)進(jìn)行,要熟記有關(guān)物質(zhì)的溶解性及顏色,以便靈活應(yīng)用.
12.能除去KNO3和NaCl混合液中所含有少量CuSO4和Fe2(SO4)3的一種試劑是( )
A.Ba(OH)2????????????? B.BaCl2????????????? C.AgNO3????????????? D.NaOH
【考點(diǎn)】2H:物質(zhì)除雜或凈化的探究;9H:鹽的化學(xué)性質(zhì).
【專題】533:物質(zhì)的分離、除雜、提純與共存問(wèn)題.
【分析】根據(jù)原物質(zhì)和雜質(zhì)的性質(zhì)選擇適當(dāng)?shù)某s劑和分離方法,所謂除雜(提純),是指除去雜質(zhì),同時(shí)被提純物質(zhì)不得改變.除雜質(zhì)題至少要滿足兩個(gè)條件:①加入的試劑只能與雜質(zhì)反應(yīng),不能與原物質(zhì)反應(yīng);②反應(yīng)后不能引入新的雜質(zhì).
【解答】解:A、CuSO4、Fe2(SO4)3分別能與Ba(OH)2反應(yīng)生成硫酸鋇沉淀和氫氧化銅沉淀、硫酸鋇沉淀和氫氧化鐵沉淀,能除去雜質(zhì)且沒(méi)有引入新的雜質(zhì),符合除雜原則,故選項(xiàng)所采取的方法正確.
B、CuSO4、Fe2(SO4)3分別能與BaCl2反應(yīng)生成硫酸鋇沉淀和氯化銅、硫酸鋇沉淀和氯化鐵,能除去雜質(zhì)但引入了新的雜質(zhì)氯化銅、氯化鐵,不符合除雜原則,故選項(xiàng)所采取的方法錯(cuò)誤.
C、NaCl能與AgNO3溶液反應(yīng)生成氯化銀沉淀和硝酸,反而會(huì)把原物質(zhì)除去,不符合除雜原則,故選項(xiàng)所采取的方法錯(cuò)誤.
D、CuSO4、Fe2(SO4)3分別能與NaOH溶液反應(yīng)生成氫氧化銅沉淀和硫酸鈉、氫氧化鐵沉淀和硫酸鈉,能除去雜質(zhì)但引入了新的雜質(zhì)硫酸鈉,不符合除雜原則,故選項(xiàng)所采取的方法錯(cuò)誤.
故選:A.
【點(diǎn)評(píng)】物質(zhì)的分離與除雜是中考的重點(diǎn),也是難點(diǎn),解決除雜問(wèn)題時(shí),抓住除雜質(zhì)的必需條件(加入的試劑只與雜質(zhì)反應(yīng),反應(yīng)后不能引入新的雜質(zhì))是正確解題的關(guān)鍵.
13.為了驗(yàn)證Fe、Cu、Ag三種金屬的活動(dòng)性順序,現(xiàn)有所需金屬,如果只選一種鹽且實(shí)驗(yàn)最簡(jiǎn)單的是( )
A.AgNO3????????????? B.CuSO4????????????? C.FeSO4????????????? D.ZnCl2
【考點(diǎn)】86:金屬活動(dòng)性順序及其應(yīng)用.
【專題】524:金屬與金屬材料.
【分析】根據(jù)金屬活動(dòng)性順序進(jìn)行分析,驗(yàn)證三種金屬活動(dòng)性強(qiáng)弱關(guān)系時(shí),通常采取“三取中”即:取中間金屬單質(zhì)與兩端的金屬的鹽溶液反應(yīng)或取中間金屬的鹽溶液與兩端金屬的單質(zhì)反應(yīng).
【解答】解:A、Fe,Cu,AgNO3溶液三種物質(zhì)中,鐵、銅都能與AgNO3溶液反應(yīng),證明鐵和銅都活動(dòng)性比銀的活動(dòng)性強(qiáng),但無(wú)法比較鐵和銅但活動(dòng)性順序,所以此方案不可行;
B、鐵可以置換CuSO4溶液中的銅而出現(xiàn)紅色固體,證明鐵的活動(dòng)性比銅強(qiáng),銀和CuSO4溶液不反應(yīng),證明銅比銀的活動(dòng)性強(qiáng),因此,可以證明三種金屬的活動(dòng)性強(qiáng)弱,此方案可行且實(shí)驗(yàn)最簡(jiǎn)單;
C、Fe的活動(dòng)性在三種金屬中最強(qiáng),所以Cu,Ag都不能和FeSO4溶液反應(yīng),得不出Cu,Ag的活動(dòng)性強(qiáng)弱,所以此方案不可行;
D、三種金屬都不能和氯化鋅反應(yīng),無(wú)法比較三種金屬都活動(dòng)性順序,所以此方案不可行;
故選項(xiàng)為:B.
【點(diǎn)評(píng)】本題考查了金屬活動(dòng)性順序的應(yīng)用,同學(xué)們要會(huì)利用金屬活動(dòng)順序表設(shè)計(jì)實(shí)驗(yàn)、選擇試劑,去驗(yàn)證金屬的活動(dòng)性強(qiáng)弱.
14.工業(yè)鹽酸因含有FeCl3而顯黃色,現(xiàn)向1~2ml工業(yè)鹽酸中逐滴滴加NaOH溶液,其加入量(X)與生成沉淀量(Y)的關(guān)系應(yīng)是( )
A.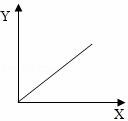 ????????????? B.
????????????? B.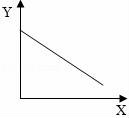 ????????????? C.
????????????? C.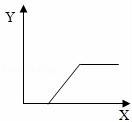 ????????????? D.
????????????? D.
【考點(diǎn)】95:堿的化學(xué)性質(zhì);93:酸的化學(xué)性質(zhì).
【專題】137:實(shí)驗(yàn)操作型;174:圖表分析,尋找有效數(shù)據(jù);526:常見(jiàn)的堿 堿的通性.
【分析】因氫氧化鐵和鹽酸先反應(yīng)能生成氯化鐵和水,鹽酸反應(yīng)完畢后氯化鐵和氫氧化鈉反應(yīng)能生成氫氧化鐵沉淀和氯化鈉,根據(jù)反應(yīng)特點(diǎn)尋找符合題意的圖象.
【解答】解:向工業(yè)鹽酸中逐滴加入NaOH溶液時(shí),因?yàn)闅溲趸c能和鹽酸反應(yīng),所以開(kāi)始沒(méi)有沉淀產(chǎn)生,當(dāng)氫氧化鈉把鹽酸消耗完后,才開(kāi)始產(chǎn)生沉淀,當(dāng)氯化鐵消耗完后,不再產(chǎn)生沉淀,C圖符合變化規(guī)律.
故選C.
【點(diǎn)評(píng)】本題主要考查各種物質(zhì)的性質(zhì)方面的知識(shí),解答時(shí)要把物質(zhì)的性質(zhì)和圖中信息結(jié)合起來(lái)進(jìn)行分析、判斷,從而得出正確的結(jié)論.
15.(南充市中考化學(xué))鐵有三種常見(jiàn)的氧化物:FeO、Fe2O3、Fe3O4.現(xiàn)有某鐵的氧化物樣品,已知其中鐵與氧質(zhì)量比是21:8關(guān)于該樣品的說(shuō)法正確的是( )
A.一定是純凈物
B.一定是混合物
C.不可能是Fe3O4和FeO組成的混合物
D.該樣品只有兩種情況,即只有Fe3O4或者是FeO、Fe2O3構(gòu)成的混合物
【考點(diǎn)】D9:元素質(zhì)量比的計(jì)算.
【專題】191:化學(xué)式的計(jì)算.
【分析】首先計(jì)算三種物質(zhì)中鐵氧兩種元素的質(zhì)量比,將所得三個(gè)數(shù)據(jù)與題目中所給數(shù)據(jù)21:8進(jìn)行比較,若為一種純凈物,則該物質(zhì)中鐵氧兩元素的質(zhì)量比值為21:8;若為混合物,則混合物中各物質(zhì)的鐵氧質(zhì)量比必須有大于21:8,也必須有小于21:8;進(jìn)行解答.
【解答】解:FeO中鐵元素與氧元素的質(zhì)量比為:56:16=7:2;
Fe2O3中鐵元素與氧元素的質(zhì)量比為:(56×2):(16×3)=7:3;
Fe3O4中鐵元素與氧元素的質(zhì)量比為:(56×3):(16×4)=21:8;
經(jīng)計(jì)算得 7:2>21:8>7:3,
若該物質(zhì)為純凈物,則只能為四氧化三鐵;
若為混合物則可以是FeO,F(xiàn)e2O3的混合物;也可以是Fe3O4,F(xiàn)eO,F(xiàn)e2O3三者的混合物,所以此題有三種可能性;由此可判斷:
A、一定是純凈物,說(shuō)法錯(cuò)誤;
B、一定是混合物,說(shuō)法錯(cuò)誤;
C、不可能是Fe3O4和FeO組成的混合物,說(shuō)法正確;
D、該樣品有三種情況,即只有Fe3O4或者是FeO、Fe2O3構(gòu)成的混合物或者是三種物質(zhì)的混合物,說(shuō)法錯(cuò)誤;
故選C.
【點(diǎn)評(píng)】本題考查學(xué)生對(duì)元素質(zhì)量比的計(jì)算及平均值法的運(yùn)用,解此類題時(shí),質(zhì)量比的計(jì)算要準(zhǔn)確,理解平均值法的含義,明確比較方法是解題的關(guān)鍵.
二、填空題
16.用符號(hào)表示:(1)兩個(gè)亞鐵離子 2Fe2+ ;(2)3個(gè)硫酸分子 3H2SO4 .
【考點(diǎn)】DF:化學(xué)符號(hào)及其周圍數(shù)字的意義.
【專題】152:結(jié)合課本知識(shí)的信息;513:化學(xué)用語(yǔ)和質(zhì)量守恒定律.
【分析】(1)根據(jù)離子的表示方法:在表示該離子的元素符號(hào)右上角,標(biāo)出該離子所帶的正負(fù)電荷數(shù),數(shù)字在前,正負(fù)符號(hào)在后,帶1個(gè)電荷時(shí),1要省略.若表示多個(gè)該離子,就在其元素符號(hào)前加上相應(yīng)的數(shù)字;進(jìn)行解答;
(2)根據(jù)分子的表示方法:正確書(shū)寫(xiě)物質(zhì)的化學(xué)式,表示多個(gè)該分子,就在其化學(xué)式前加上相應(yīng)的數(shù)字,進(jìn)行解答.
【解答】解:(1)根據(jù)離子的表示方法:在表示該離子的元素符號(hào)右上角,標(biāo)出該離子所帶的正負(fù)電荷數(shù),數(shù)字在前,正負(fù)符號(hào)在后,帶1個(gè)電荷時(shí),1要省略.若表示多個(gè)該離子,就在其元素符號(hào)前加上相應(yīng)的數(shù)字;因此兩個(gè)亞鐵離子表示為:2Fe2+;故答案為:2Fe2+;
(2)根據(jù)分子的表示方法:正確書(shū)寫(xiě)物質(zhì)的化學(xué)式,表示多個(gè)該分子,就在其化學(xué)式前加上相應(yīng)的數(shù)字,因此3個(gè)硫酸分子表示為:3H2SO4;故答案為:3H2SO4.
【點(diǎn)評(píng)】本題主要考查學(xué)生對(duì)化學(xué)用語(yǔ)的書(shū)寫(xiě)和理解能力,題目設(shè)計(jì)既包含對(duì)化學(xué)符號(hào)意義的了解,又考查了學(xué)生對(duì)化學(xué)符號(hào)的書(shū)寫(xiě),考查全面,注重基礎(chǔ).
17.硒元素具有抗衰老,抑制癌細(xì)胞的功能,它的化學(xué)性質(zhì)與硫相似,元素符號(hào)為Se,它對(duì)應(yīng)的含氧酸的化學(xué)式是:H2SeO4,這種酸應(yīng)讀作 硒酸 ,其與氫氧化鈉溶液反應(yīng)的化學(xué)方程式是 H2SeO4+2NaOH=Na2SO4+2H2O .
【考點(diǎn)】93:酸的化學(xué)性質(zhì);G5:書(shū)寫(xiě)化學(xué)方程式.
【專題】525:常見(jiàn)的酸 酸的通性.
【分析】運(yùn)用酸的命名、堿能和酸反應(yīng)生成鹽和水解答
【解答】解:含氧酸以除氫元素、氧元素外的第三種元素的名稱命名為某酸,H2SeO4中除氫元素、氧元素外的第三種元素是硒,故是硒酸.
硒酸和氫氧化鈉反應(yīng)生成硒酸鈉和水,故答案:H2SeO4+2NaOH=Na2SeO4+2H2O
【點(diǎn)評(píng)】此題借助生活中的一些常見(jiàn)物質(zhì)對(duì)不同物質(zhì)的性質(zhì)進(jìn)行了考查,解題時(shí)只要掌握各物質(zhì)之間的反應(yīng)即可順利解題.
18.如圖為香煙中有害物質(zhì)尼古丁的結(jié)構(gòu)式(短線代表電子對(duì)),則該物質(zhì)的化學(xué)式為 C10H14N2 ,該物質(zhì)的相對(duì)分子質(zhì)量為 162 .
【考點(diǎn)】D8:相對(duì)分子質(zhì)量的概念及其計(jì)算;D1:化學(xué)式的書(shū)寫(xiě)及意義.
【專題】191:化學(xué)式的計(jì)算.
【分析】根據(jù)圖示中尼古丁的結(jié)構(gòu)式,查出尼古丁分子中碳原子、氫原子、氮原子的個(gè)數(shù),確定化學(xué)式,然后計(jì)算相對(duì)分子質(zhì)量,相對(duì)分子質(zhì)量為各種元素的總質(zhì)量;
【解答】解:由示意圖知,一個(gè)分子中含有10個(gè)碳原子,14個(gè)氫原子和兩個(gè)氮原子,故化學(xué)式為C10H14N2;相對(duì)分子質(zhì)量=(12×10)+(1×14)+(14×2)=162;
故答案為:C10H14N2;162.
【點(diǎn)評(píng)】能根據(jù)結(jié)構(gòu)式確定分子的構(gòu)成,掌握化學(xué)式的書(shū)寫(xiě)及意義、物質(zhì)的元素組成;掌握相對(duì)分子質(zhì)量的概念及其計(jì)算.
19.蛋糕等食品包裝中的除氧劑是一種黑色粉末狀的固體,失效后帶有紅褐色.某化學(xué)課外興趣小組為了探究其主要成分,將一包未變質(zhì)的除氧劑分成兩份:一份加入稀鹽酸中,發(fā)現(xiàn)大量氣泡產(chǎn)生;另一份加入到氯化銅溶液中,一段時(shí)間后溶液顏色變淡綠色,固體逐漸變紅.請(qǐng)回答:
(1)該除氧劑的主要成份是 Fe ;
(2)為了驗(yàn)證上述推斷是否正確,可以用到一種物理方法,即 用磁鐵吸此除氧劑,如果此黑色粉末被吸引,則證明此除氧劑為鐵粉 .
【考點(diǎn)】(南充市中考化學(xué))2D:食品干燥劑、保鮮劑和真空包裝的成分探究;81:常見(jiàn)金屬的特性及其應(yīng)用;85:金屬的化學(xué)性質(zhì).
【專題】537:科學(xué)探究.
【分析】(1)鐵能與水和氧氣作用生成鐵銹的性質(zhì)解答;
(2)鐵能被磁鐵吸引.
【解答】解:
(1)鐵能與水和氧氣反應(yīng)生成鐵銹,故用除氧劑;
(2)鐵能被磁鐵吸引,為了驗(yàn)證上述推斷是否正確,可以用到一種物理方法是用磁鐵吸引.
答案:
(1)Fe;
(2)用磁鐵吸此除氧劑,如果此黑色粉末被吸引,則證明此除氧劑為鐵粉.
【點(diǎn)評(píng)】解答本題的關(guān)鍵是要掌握物質(zhì)的性質(zhì)和用途等方面的知識(shí),只有這樣才能對(duì)問(wèn)題做出正確的判斷.
20.如圖是a、b兩種固體物質(zhì)的溶解度曲線,試回答:
(1)t℃時(shí),兩物質(zhì)的溶解度的大小關(guān)系:a 大于 b(填“大于”、“等于”或“小于”)
(2)當(dāng)a中含有 少量b時(shí),可以用 降溫結(jié)晶 法提純a;
(3)a、b都屬于 易溶 物質(zhì);(填“難溶”、“微溶”、“可溶”、“易溶”)
(4)在 20 ℃時(shí)a、b的溶解度相等,此時(shí)150g水中最多可溶解物質(zhì) 30 g.
【考點(diǎn)】7N:固體溶解度曲線及其作用;4H:結(jié)晶的原理、方法及其應(yīng)用;7Q:物質(zhì)的溶解性及影響溶解性的因素.
【專題】515:溶液、濁液與溶解度.
【分析】根據(jù)固體物質(zhì)溶解度曲線的意義,可以比較不同物質(zhì)在同一溫度下的溶解度大小,判斷物質(zhì)的溶解度隨溫度變化的變化情況,從而可以判斷出提純物質(zhì)的方法等,溶解度曲線上的各點(diǎn)表示該物質(zhì)在不同溫度下的溶解度,可以根據(jù)溶解度進(jìn)行有關(guān)的計(jì)算;按照在20℃時(shí)的物質(zhì)溶解度的大小把物質(zhì)分為了四類:①易溶物質(zhì)(>10g),②可溶物質(zhì)(>1g),③微溶物質(zhì)(>0.01g),④難溶物質(zhì)(<0.01g).
【解答】解:(1)從溶解度曲線上可以看出在t℃時(shí),a的溶解度大于b的溶解度;
(2)從溶解度曲線上可以看出,a的溶解度受溫度的影響較大,而b的溶解度受溫度的影響較小,所以當(dāng)a中含有少量b時(shí),可以采取冷卻熱飽和溶液的方法提純a;
(3)由于兩物質(zhì)的溶解度在20℃時(shí)都大于10g,都應(yīng)屬于易溶物質(zhì);
(4)由溶解度曲線的意義可以知道:溶解度曲線的交點(diǎn)為幾種物質(zhì)在該溫度下的溶解度相等的時(shí)候,所以可以判斷在溫度為20℃時(shí),a、b的溶解度相等為20g,根據(jù)溶解度的意義可以知道150g水中能夠溶解30ga物質(zhì).
故答為:(1)大于;(2)降溫結(jié)晶;(3)易溶;(4)20,30.
【點(diǎn)評(píng)】本題難度不大,主要考查了根據(jù)固體物質(zhì)的溶解度曲線來(lái)解決相關(guān)的問(wèn)題,加深學(xué)生對(duì)固體溶解度的理解.
21.現(xiàn)有一包白色固體混合物,可能由BaCl2、KNO3、CuSO4、FeCl3、Na2CO3、Na2SO4、NaCl等中的幾種混合而成,為證明其組成,做如下實(shí)驗(yàn):
①取一定量該固體混合物加入足量的水,充分?jǐn)嚢瑁玫桨咨恋砗蜔o(wú)色溶液.過(guò)濾得到白色沉淀A,無(wú)色濾液B.
②向白色沉淀A中加入過(guò)量的鹽酸溶液,沉淀部分溶解.
③向無(wú)色濾液B中加入硝酸銀溶液,產(chǎn)生不溶于稀硝酸的白色沉淀.
則:(1)該固體混合物中一定含有 BaCl2、Na2CO3、Na2SO4 ,可能含有 KNO3、NaCl ,一定沒(méi)有 CuSO4、FeCl3 .(用化學(xué)式填空)
(2)該混合物至少由 3 種物質(zhì)構(gòu)成,該混合物的所有可能組合有 4 種(填數(shù)字).
【考點(diǎn)】AE:物質(zhì)的鑒別、推斷;E7:反應(yīng)現(xiàn)象和本質(zhì)的聯(lián)系.
【專題】114:混合物組成的推斷題.
【分析】(1)由題意知“得到白色沉淀和無(wú)色溶液”,又因?yàn)榱蛩徙~溶液為藍(lán)色,氯化鐵溶液為黃色,所以一定沒(méi)有硫酸銅和氯化鐵;
(2)“向白色沉淀A中加入過(guò)量的鹽酸溶液,沉淀部分溶解”說(shuō)明有碳酸根、硫酸根、鋇離子;
(3)“向無(wú)色濾液B中加入硝酸銀溶液,產(chǎn)生不溶于稀硝酸的白色沉淀”說(shuō)明無(wú)色濾液B中含有氯離子.
(4)KNO3、NaCl不能確定是否含有.
【解答】解:(1)①白色沉淀A遇過(guò)量的鹽酸溶液,部分溶解,所以一定含有BaCl2、Na2CO3、Na2SO4;②KNO3、NaCl不能確定是否含有;③混合物溶于水,得沉淀和無(wú)色溶液,所以一定沒(méi)有CuSO4、FeCl3.
(2)①該混合物至少由3種物質(zhì)組成,即一定含有BaCl2、Na2CO3、Na2SO4;
②該混合物的所有可能組合:A、BaCl2、Na2CO3、Na2SO4、B、BaCl2、Na2CO3、Na2SO4、KNO3、
C、BaCl2、Na2CO3、Na2SO4、NaCl、D、BaCl2、Na2CO3、Na2SO4、KNO3、NaCl
故答為:(1)一定含BaCl2、Na2CO3、Na2SO4;可能含KNO3、NaCl;一定沒(méi)CuSO4、FeCl3
(2)3種、4種
【點(diǎn)評(píng)】掌握物質(zhì)的反應(yīng)現(xiàn)象和本質(zhì)的聯(lián)系,解題時(shí)往往需要從題目中挖出一些明顯或隱含的條件,抓住突破口,導(dǎo)出結(jié)論,最后別忘了把結(jié)論代入原題中驗(yàn)證,若“路”走得通則已經(jīng)成功.
三、(南充市中考化學(xué))實(shí)驗(yàn)題
22.現(xiàn)有一定量的含ZnO的鋅粒,請(qǐng)從圖中選擇適當(dāng)?shù)膶?shí)驗(yàn)裝置,設(shè)計(jì)一實(shí)驗(yàn)測(cè)定鋅粒的純度,可供選擇的試劑有:①稀硫酸 ②稀硝酸 ③濃硫酸 ④硫酸銅溶液 ⑤濃硝酸.
請(qǐng)回答下列問(wèn)題:
(1)寫(xiě)出儀器的名稱:1 鐵架臺(tái) 2 長(zhǎng)頸漏斗 3 試管 ;
(2)測(cè)定純度可以設(shè)計(jì)兩種方法,一種是最簡(jiǎn)單的,則選擇儀器是 戊乙丙 (填裝置編號(hào)).戊中選擇的藥品是 ① (填編號(hào));若氣體從左向右流,則接口的順序?yàn)椤→D→C→E (填接口字母代號(hào));
(3)儀器組裝好后,在開(kāi)始實(shí)驗(yàn)時(shí),要先 檢驗(yàn)裝置氣密性 ,操作方法是 用手堵塞導(dǎo)管口向長(zhǎng)頸漏斗中倒水,直到長(zhǎng)頸漏斗中有液柱差,說(shuō)明裝置不漏氣 .
(4)若實(shí)驗(yàn)樣品質(zhì)量是10g,實(shí)驗(yàn)中測(cè)定氫氣的體積是2.22L(氫氣密度為0.09g/L)則樣品的純度為 65% .
【考點(diǎn)】HK:氫氣的化學(xué)性質(zhì)與燃燒實(shí)驗(yàn);4R:氣體的凈化(除雜);7V:氫氣的制取和檢驗(yàn);G5:書(shū)寫(xiě)化學(xué)方程式.
【專題】164:綜合實(shí)驗(yàn)題.
【分析】(1)認(rèn)識(shí)常見(jiàn)儀器的名稱;
(2)根據(jù)鋅和稀硫酸反應(yīng)生成氫氣,氫氣難溶于水進(jìn)行解答;
(3)根據(jù)有氣體生成的反應(yīng)要先檢驗(yàn)裝置的氣密性進(jìn)行解答;
(4)根據(jù)氫氣的體積求出氫氣的質(zhì)量,從而求出氫氣的質(zhì)量,利用氫氣的質(zhì)量求出金屬鋅的質(zhì)量即可.
【解答】解:(1)熟悉常用化學(xué)儀器的名稱,分別為鐵架臺(tái),長(zhǎng)頸漏斗,試管;故填:鐵架臺(tái),長(zhǎng)頸漏斗,試管;
(2)鋅和稀硫酸反應(yīng)生成氫氣,氫氣難溶于水,排出水的體積就等于氫氣的體積,所以測(cè)定純度可選擇儀器是戊乙丙,戊中選擇的藥品是稀硫酸;若氣體從左向右流,則接口的順序?yàn)镠→D→C→E;故填:戊乙丙;①;H→D→C→E;
(3)有氣體生成的反應(yīng)要先檢驗(yàn)裝置的氣密性,操作方法是用手堵塞導(dǎo)管口向長(zhǎng)頸漏斗中倒水,直到長(zhǎng)頸漏斗中有液柱差,說(shuō)明裝置不漏氣;故填:檢驗(yàn)裝置氣密性;用手堵塞導(dǎo)管口向長(zhǎng)頸漏斗中倒水,直到長(zhǎng)頸漏斗中有液柱差,說(shuō)明裝置不漏氣;
(4)氫氣的質(zhì)量=2.22L×0.09g/L≈0.2g
設(shè)樣品中鋅的質(zhì)量為x
Zn+H2SO4=ZnSO4+H2↑??
65?????????????? 2
x?? ? ? 0.2g
![]()
x=6.5g
樣品的純度=![]() =65%
=65%
答:樣品的純度為65%.
故填:65%.
【點(diǎn)評(píng)】此題是對(duì)實(shí)驗(yàn)裝置的設(shè)計(jì)考查題,解題的關(guān)鍵是對(duì)實(shí)驗(yàn)?zāi)康囊蟮膯?wèn)題進(jìn)行設(shè)計(jì),并結(jié)合相關(guān)的化學(xué)方程式的計(jì)算對(duì)實(shí)驗(yàn)數(shù)據(jù)進(jìn)行分析探討.
四、計(jì)算題
23.某石灰廠新到一批石灰石,其中含有雜質(zhì)二氧化硅(二氧化硅不溶于水,不與鹽酸反應(yīng),高溫不分解)為測(cè)定石灰石樣品的純度,某化學(xué)研究性學(xué)習(xí)小組的同學(xué)分成三組實(shí)驗(yàn)測(cè)得數(shù)據(jù)如表:
實(shí)驗(yàn)次數(shù) | 1 | 2 | 3 |
稀鹽酸質(zhì)量(g) | 50 | 50 | 100 |
樣品質(zhì)量(g) | 20 | 30 | 20 |
剩余物質(zhì)質(zhì)量(g) | 63.4 | 73.4 | 113.4 |
產(chǎn)生氣體的質(zhì)量(g) | 6.6 | 6.6 |
|
(1)表格第3組空格中應(yīng)填寫(xiě)的數(shù)據(jù)是 6.6 ;
(2)該實(shí)驗(yàn)中,第 1、2 (填數(shù)字)組同學(xué)的實(shí)驗(yàn)中,稀鹽酸一定反應(yīng)完全;
(3)求出該石灰石樣品的純度. (請(qǐng)寫(xiě)出計(jì)算過(guò)程,否則不得分)
【考點(diǎn)】G6:根據(jù)化學(xué)反應(yīng)方程式的計(jì)算.
【專題】193:有關(guān)化學(xué)方程式的計(jì)算.
【分析】(1)根據(jù)質(zhì)量守恒定律,判斷第3次實(shí)驗(yàn)所得到氣體的質(zhì)量;
(2)對(duì)三組實(shí)驗(yàn)數(shù)據(jù)進(jìn)行分析,通過(guò)對(duì)比稀鹽酸質(zhì)量、樣品質(zhì)量、產(chǎn)生氣體的質(zhì)量三者間的關(guān)系,判斷反應(yīng)進(jìn)度及反應(yīng)物剩余情況;
(3)利用第1或3組碳酸鈣完全反應(yīng)所得實(shí)驗(yàn)數(shù)據(jù),根據(jù)反應(yīng)的化學(xué)方程式,由產(chǎn)生二氧化碳質(zhì)量計(jì)算樣品中所含碳酸鈣質(zhì)量,求出該石灰石樣品的純度.
【解答】解:(1)根據(jù)質(zhì)量守恒定律,第3次實(shí)驗(yàn)所得到氣體的質(zhì)量=100g+20g﹣113.4g=6.6g;故填:6.6;
(2)對(duì)比實(shí)驗(yàn)1、2,當(dāng)樣品質(zhì)量增加時(shí),放出二氧化碳質(zhì)量并未增加,說(shuō)明實(shí)驗(yàn)中稀鹽酸已完全反應(yīng);對(duì)比實(shí)驗(yàn)1、3,當(dāng)稀鹽酸質(zhì)量增加時(shí),放出二氧化碳的質(zhì)量不變,說(shuō)明實(shí)驗(yàn)中碳酸鈣已完全反應(yīng);綜上所述,20g樣品能恰好和50g鹽酸反應(yīng);故填:1、2;
(3)設(shè)20g樣品中碳酸鈣的質(zhì)量為x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100???????? ?? ???? 44
x???????????????????? 6.6g
![]()
x=15g
則該石灰石樣品的純度為![]() ×100%=75%
×100%=75%
答:該石灰石樣品的純度為75%.
【點(diǎn)評(píng)】石灰石的主要成分為碳酸鈣,因此石灰石樣品的純度即主要成分碳酸鈣在樣品中的質(zhì)量分?jǐn)?shù),即樣品中所含碳酸鈣質(zhì)量與樣品的質(zhì)量比.

孔乙己是貧困潦倒的知識(shí)分子。在書(shū)中,孔乙己是一個(gè)知識(shí)分子,滿口“之乎者也”,但是他很窮,還竊書(shū),說(shuō)過(guò)“讀書(shū)人的事,怎么能叫竊,”被人嘲笑,他...

自然界產(chǎn)生氧氣的化學(xué)方程式:光合作用的反應(yīng)式為6CO2+12H2O→C6H12O6+6O2+6H2O。包括光反應(yīng)和暗反應(yīng)兩個(gè)過(guò)程。需要具備光...

有的高校沒(méi)有條件,只要學(xué)業(yè)水平成績(jī)都合格就可以,比如中國(guó)科學(xué)院大學(xué)。有的需要平常學(xué)習(xí)考試成績(jī),比如北京外國(guó)語(yǔ)大學(xué)要求高三第一學(xué)期期末成績(jī)?cè)谌?..

在四則運(yùn)算中,表示計(jì)算順序,在小括號(hào)之后、大括號(hào)之前;表示兩個(gè)整數(shù)的最小公倍數(shù);表示取未知數(shù)的整數(shù)部分;在函數(shù)中,表示函數(shù)的閉區(qū)間;在線性代...

濟(jì)南開(kāi)設(shè)的最好的職高學(xué)校有:濟(jì)南方信集團(tuán)職業(yè)高中、濟(jì)南公共交通職業(yè)高中。濟(jì)南市公共交通職業(yè)高級(jí)中學(xué)是由濟(jì)南市公共交通總公司承辦,業(yè)務(wù)屬濟(jì)南市...

實(shí)然:是說(shuō)事物實(shí)際上就是這樣的,但不同于現(xiàn)實(shí)性(現(xiàn)實(shí)性指其有合理性和客觀性);應(yīng)然:就是應(yīng)該是怎么樣的意思,比如說(shuō)這件事,就應(yīng)該是那樣的結(jié)果...

地中海氣候一種夏季炎熱干燥、冬季溫和多雨,雨熱不同期的氣候類型。地中海氣候冬季受西風(fēng)帶控制,鋒面氣旋頻繁活動(dòng),氣候溫和,最冷月的氣溫在4-1...

堿石灰,又稱鈉石灰,堿石灰是白色或米黃色粉末,疏松多孔,是氧化鈣(CaO,大約75%),水(H?O,大約20%),氫氧化鈉(NaOH,大約3...